Personalisierte Medizin
Die Bevölkerung in Deutschland lebt immer länger: Die Lebenserwartung ist in den letzten zwanzig Jahren von 78 auf 81 Jahre gestiegen. Damit verbunden sind jedoch auch erhebliche und kontinuierlich steigende Gesundheitsausgaben. Denn je älter die Menschen werden, desto häufiger treten meist multiple chronische Krankheiten und altersbedingte Funktionsdefizite auf. Der einzelne Patient wird zu einem komplexen klinischen Mosaik, das die traditionelle Medizin auch durch zunehmende Kosten vor Herausforderungen stellt.
Die Digitalisierung öffnet bei einer großen Zahl von Krankheitsbildern Forschungs- und Anwendungspotenziale, um Prävention, Diagnostik und Therapie zu verbessern. Die Analyse großer klinischer und molekularer Datensätze (Big Data) kann einen wichtigen Beitrag zu einer personalisierten, auf den Einzelnen ausgerichteten Medizin leisten und dabei möglicherweise sogar Kosten senken. Wir stellen einige Forschungsprojekte vor, die das Potential aufzeigen, das sich aus der Analyse großer Datenmengen im biomedizinischen Bereich für die personalisierte Medizin ergibt.

KI-Servicezentrum für kritische und sensible Infrastrukturen (KISSKI)
KI-Service für Medizin und Gesundheitswesen
Im medizinischen Bereich werden hohe Anforderungen an den Einsatz von KI-Methoden gestellt, da es sich bei der Medizin um eine sensible und kritische Infrastruktur handelt. Dies betrifft z.B. garantierte Antwortzeiten, hohe Anforderungen an die Datensicherheit, Resilienz gegenüber Cyberangriffen sowie die Interpretierbarkeit von KI-Modellen. Vor diesem Hintergrund will das Servicezentrum KISSKI die Frage beantworten, wie KI-Modelle für kritische Infrastrukturen effektiv in diese anspruchsvolle Praxis überführt werden können.
Durch die zunehmende Komplexität der Aufgabenstellungen sowie die Verfügbarkeit immer größerer Datenmengen durch neue Sensorik und Aktorik in der Medizin besitzen KI-Methoden ein großes Potenzial.
Insbesondere für kleine und mittelständische Unternehmen, aber auch für größere Unternehmen und Institutionen stellen Investitionen in die notwendige Hardware-Infrastruktur und der Zugang zu Expertenwissen eine große Herausforderung bei der Anwendung von KI Technologien dar. Ein zentrales Anliegen von KISSKI ist es daher, einen effektiven Zugang zu KI-Infrastruktur, -Methoden und -Expertise zu ermöglichen.
Die KISSKI KI-Servicezentren bieten umfassende Dienstleistungen an, um KI-Methoden und Expertenwissen für die praktische Anwendung zugänglich zu machen. Zielgruppen sind unter anderem Institutionen wie Universitätskliniken und Krankenhäuser, Krankenkassen, Kassenärztliche Vereinigungen sowie medizinische Forschungseinrichtungen. Darüber hinaus richten sich die Angebote an KMU und Start-ups aus den Bereichen Biotechnologie, Pharma, Medizintechnik und Digital Healthcare.

Globale Kooperation auf dem Weg zur personalisierten Medizin
Jeder Mensch ist einzigartig. Auch im Bereich der Medizin gibt es daher nicht immer die eine allgemeingültige Lösung für jeden. Künstliche Intelligenz bietet die Möglichkeit, Medizin zu personalisieren und individuell auf jeden Patienten eingehen zu können.
Personalisierte Medizin stellt den Patienten in den Mittelpunkt Prävention, Diagnostik und Therapie werden dabei auf die individuellen Bedürfnisse des Einzelnen abgestimmt. Um das alles leisten zu können, müssen riesige Datenmengen verarbeitet und analysiert werden. Dies erfordert intelligente, zuverlässige und verantwortungsvolle Systeme.
Seit Mai 2020 arbeiten im Leibniz-Zukunftslabor für Künstliche Intelligenz (LeibnizAILab) exzellente Forscher aus aller Welt mit Kollegen der Leibniz Universität, der Medizinischen Hochschule Hannover (MHH) und europäischer Partnerinstitute zusammen, solche Systeme für die personalisierte Medizin zu entwickeln. Das interdisziplinäre Forschungsteam integriert eine Vielzahl von Ansätzen, die für KI relevant sind. Es ist wichtig, dass die Verfahren sowohl reproduzierbar als auch robust sind und der Datenschutz immer gewährleistet ist. Die Ergebnisse intelligenter Systeme müssen erklärbar, fair und zurechenbar sein.
Aktuell wird in vier Anwendungsfällen geforscht: Brustkrebs, psychiatrische Erkrankungen, Leukämie und Organversagen auf der Kinderintensivstation.
Video © Bundesministerium für Bildung und Forschung (BMBF)
Leibniz KI Labor
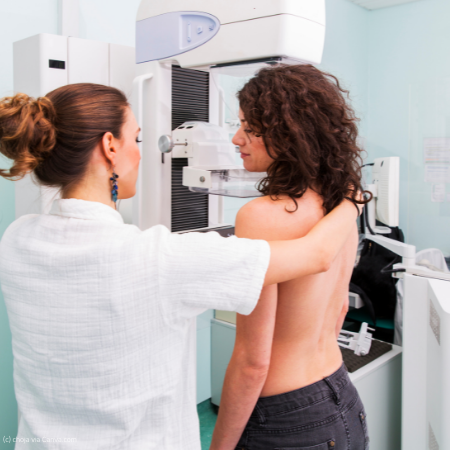
Use Case: Brustkrebs
Ziel des Projekts ist die Entwicklung von KI-Methoden zur Aufdeckung individueller Merkmale, die sich auf den Therapieerfolg von Patientinnen mit Brustkrebs auswirken können. Die KI-Methoden stützen sich auf ein ganzheitliches Profil von Brustkrebspatientinnen, um genaue und erklärbare Prognosen über den Krankheitsverlauf zu erstellen und so eine individualisierte Behandlung zu unterstützen.
Brustkrebs ist eine heterogene Krankheit, die sich bei einzelnen Patientinnen unterschiedlich äußert, was eine individuelle Behandlung schwierig macht. Bestehende Ansätze beruhen auf spezifischen Patientenmerkmalen (z.B. die medizinische oder genetische Vorgeschichte). Die Integration verschiedener Arten von Patientendaten (z.B. sozioökonomische, pharmakogenetische und familiäre Daten) kann aber eine ganzheitliche und interpretierbare Analyse von Brustkrebspatientinnen ermöglichen.
In einer Wissensdatenbank werden Informationen zu Brustkrebspatientinnen gesammelt. Diese Datenbank integriert medizinische Aufzeichnungen, Familienanamnesen, Tumoreigenschaften, erfolgte Therapien, Nachuntersuchungen, genetische Informationen und sozioökonomische Daten. Es werden Daten von mehr als 5.000 Brustkrebspatientinnen einbezogen und analysiert. Besonderer Wert wird darauf gelegt die Zusammenhänge von sozioökonomischen Aspekten wie Bildung und Migrationshintergrund mit dem Therapieerfolg zu untersuchen. Ein weiterer Schwerpunkt ist die Identifizierung individueller Merkmale wie familiäre Krebs Vorbelastungen, Genmutationen und Lebensstile, die zusammen mit den verschiedenen Therapien, den Krankheitsverlauf und die Überlebenszeit beeinflussen können. Ethische Rahmenbedingungen bewerten die Auswirkungen von KI-Methoden auf die Patienten und die Gesellschaft; sie sind unerlässlich, um ein Einbetten oder Verstärken von Vorurteilen in die KI-Tools zu vermeiden und Transparenz zu gewährleisten. Das Forschungsteam wird von Spezialisten der Medizinischen Hochschule Hannover unterstützt. Die Projektergebnisse werden Faktoren aufdecken, die sich auf Brustkrebstherapien auswirken und zu einer neuen Art patientenzentrierter Gesundheitsversorgung beitragen.

Leibniz KI Labor
Use Case: Personalisierte Diagnostik für Leukämien
Leukämie ist die häufigste Krebserkrankung im Kindesalter. Doch trotz intensivierter Therapie stagnieren die Überlebensraten bei aggressiven Leukämien. In der klinischen Praxis sind die Genetik sowie die Leukozytenzahl und das Alter des Patienten die wichtigsten prognostischen Faktoren, die die Risikoeinstufung bestimmen. Mit der verfügbaren Diagnostik kann jedoch nicht immer eine eindeutige Aussage gemacht werden.
In den letzten Jahren haben genomweite Analysen von Leukämien unser Verständnis von pädiatrischen Leukämien enorm verbessert. Dennoch bleiben viele wichtige Fragen unbeantwortet. So ist beispielsweise in den meisten Fällen nicht bekannt, ob und wie die Markergene oder -regionen funktionell an der Krebsentstehung oder -progression beteiligt sind. Ebenso ist unklar, welche Mechanismen zu Chemotherapie Resistenz und Rückfall führen.
Das LeibnizAILab arbeitet gemeinsam mit PD Dr. Anke Bergmann vom Institut für Humangenetik (MHH) daran, diagnostische und prognostische Marker für ALL bei Kindern zu optimieren. Die Markeranalysen werden mit einem großen Datensatz durchgeführt, der vielfältige genetische Informationen mit klinischen Daten kombiniert. Genetische Daten der kindlichen Tumoren werden mittels KI analysiert, um neue Erkenntnisse zu gewinnen und die Datenanalyse zu optimieren und personalisieren. Zusätzlich ergeben sich durch die Zusammenarbeit von Datenwissenschaftlern, Medizinern, Naturwissenschaftlern und Bioinformatikern Synergien, um klinische Fragestellungen mit neuen Algorithmen zu bearbeiten und unterschiedliche medizinische, biologische und genetische Daten zu integrieren. Das Hauptziel: die Vorhersage von Veranlagung, klinischem Verlauf, Therapieerfolg und Rückfallwahrscheinlichkeit mit Hilfe künstlicher Intelligenz. Dieses Wissen ermöglicht eine gezielte Therapie, wobei die Nebenwirkungen und Langzeitfolgen individuell so gering wie möglich gehalten werden können.

Leibniz KI Labor
Use Case: Morbus Parkinson
Morbus Parkinson ist eine komplexe neurodegenerative Erkrankung mit großer Heterogenität in Bezug auf die klinischen Symptome (motorisch und nicht-motorisch), den Verlauf, das Ansprechen auf die Behandlung und genetische Faktoren. Die Subtypisierung von Patienten trägt dazu bei, die Krankheitsmechanismen besser zu verstehen, und erleichtert gezielte und individuelle Interventionen und Behandlungsverfahren.
Die Einteilung von Parkinson in Subtypen basiert bisher vorwiegend auf motorischen Symptomen, nicht-motorische Symptome werden hierbei in der Regel vernachlässigt. Allgemeine Symptom-basierte Ansätze ermöglichen kein individuelles Vorgehen und Ansätze, die darüber hinaus genetische Daten berücksichtigen, sind bisher wenig erforscht.
Unser Ziel ist es, datengesteuerte Methoden zur Subtypisierung von Patienten zu entwickeln, die sowohl motorische als auch nicht-motorische Merkmale von Parkinson integrieren und klinische und genetische Daten gemeinsam nutzen. Diese automatisch erlernten Subtypen werden untersucht, um potentielle Marker für neurodegenerative Erkrankungen wie Parkinson zu identifizieren. Mit Hilfe dieser Marker könnte ein frühzeitiges therapeutisches Eingreifen bei neurodegenerativen Erkrankungen möglich sein. Dabei arbeiten wir eng mit Experten von der Klinik für Psychiatrie, Sozialpsychiatrie und Psychotherapie der Medizinischen Hochschule Hannover (MHH) und weiteren biomedizinischen Partnern der MHH zusammen. Wir konzentrieren uns zunächst auf junge Parkinson-Patienten und Patienten mit Begleiterkrankungen wie Schizophrenie und schweren Depressionen. Unser Ziel ist es, personalisierte KI-basierte Lösungen zu entwickeln, die die Ärzte in ihrer täglichen klinischen Praxis dabei unterstützen Patienten gezielter und individueller zu diagnostizieren und zu behandeln.

Leibniz KI Labor
Use Case: Erkennung von Organfehlfunktionen in PICUs
In diesem Anwendungsfall arbeiten Ärzte der MHH gemeinsam mit dem Leibniz-KI-Labor daran, Organfehlfunktionen auf der Pädiatrischen Intensivstation (PICU) automatisch zu erkennen. Auf Intensivstationen müssen Ärzte Entscheidungen mit hohem Risiko unter großem Stress treffen. Die Datenmenge mit denen sie in diesen Situationen konfrontiert werden ist sehr umfangreich, daher ist die Entwicklung automatischer Entscheidungsfindungsmodelle mit neuesten KI-Methoden unerlässlich. Mit der Entwicklung dieser Entscheidungsfindungsmodelle, arbeiten wir auf die Entwicklung von Echtzeitmodellen hin, welche die Ärzte auf der Intensivstation unterstützen und entlasten können.
Im Vergleich zur Entwicklung von Entscheidungsmodellen bei der Verarbeitung von Daten aus Intensivstationen, gibt es weitere Schwierigkeiten bei der Entscheidungsfindung auf pädiatrischen Intensivstationen: Zum einen dominieren verschiedene Krankheiten in den Altersgruppen von 0 bis 18 Jahren, und zum anderen variieren die Normwerte in den verschiedenen Altersgruppen stark. Bisher gibt es nur wenige Forschungsstudien, die sich mit der Analyse der auf pädiatrischen Intensivstationen erhobenen Daten befassen.
In diesem Projekt arbeiten wir gemeinsam mit der Medizinischen Hochschule Hannover an dem Ziel der automatischen Vorhersage von Organfehlfunktionen auf der pädiatrischen Intensivstation. Es gibt zwei Hauptbereiche, die in diesem
Projekt geplant sind.
Zuerst werden wir uns auf die Verarbeitung der klinischen Daten konzentrieren, diese beinhalten hauptsächlich Vitalparameter (z. B. Atemfrequenz, Herzfrequenz), Laborparameter (z.B. Leukozyten), und Patientendaten (z.B. Größe,
Gewicht). Mit Hilfe neuronaler Netze werden die Organfehlfunktion aus diesen Daten vorhergesagt. Fehlende Datenpunkte sind hier nicht unüblich, Schwierigkeiten die daraus in der Vorhersage resultieren könnten, sollen
durch künstliche Vervollständigung der fehlenden Werte behoben werden. Im weiteren Verlauf des Projektes ist darüber hinaus die Verarbeitung von Wellenformdaten (z. B. Elektrokardiogramm) geplant, diese Daten werden von den
Monitoren am Patientenbett aufgenommen.
Des Weiteren unterstützt die Arbeit an Vorhersagemodellen für Organfehlfunktionen die Weiterentwicklung von Echtzeitanwendungen und andere Anwendungen von KI in der pädiatrischen Intensivstationen. Wir hoffen, dass die Anwendung
der automatischen Vorhersage von Organfehlfunktionen schon bald Leben rettet und den Stress für Ärzte und Krankenschwestern, die in der pädiatrischen Intensivstation arbeiten, reduziert.
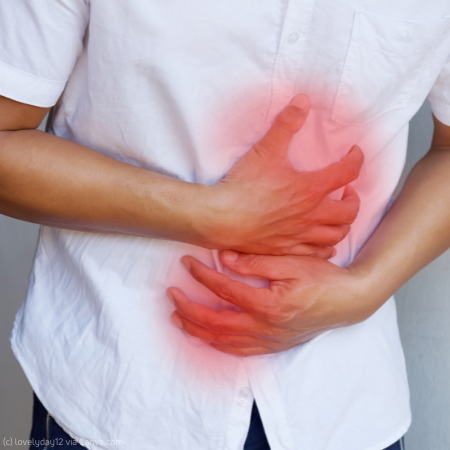
KI gegen das Norovirus
Für einen Großteil der Magen-Darm-Infekte sind Noroviren verantwortlich. Sie sind hochinfektiös und können akute Gastroenteritis-Ausbrüche in Gemeinschaftseinrichtungen, Krankenhäusern, Altenheimen oder auch auf Kreuzfahrtschiffen
auslösen. Besonders gefährlich sind Noroviren für immungeschwächte Patienten, beispielsweise nach einer Organtransplantation, da sie chronische Infektionen etablieren und Komplikationen
auslösen können.
Bisher gibt es weder einen Impfstoff noch eine spezifische Therapie zur Vorbeugung oder Behandlung von Norovirus-Infektionen. Auch ist nicht bekannt, was die individuellen Unterschiede in der Anfälligkeit und im Infektionsverlauf ausmacht.
Im Forschungsprojekt PRESENt suchen Wissenschaftler des TWINCORE, der Medizinischen Hochschule Hannover, des Helmholtz-Zentrums für Infektionsforschung und des L3S gemeinsam nach den Ursachen dieser Varianzen. In klinischen Studien werten die PRESENt-Forscher über 5000 Patientendatensätze aus. KI-Analysemethoden sollen helfen, kritische Faktoren für die Entwicklung von Komplikationen durch eine Norovirus-Infektion aufzudecken. Das Ziel ist, die Anfälligkeit jedes einzelnen Patienten für komplizierte und schwere Noroviruserkrankungen präzise und schnell vorherzusagen. Die Wissenschaftler setzen dafür klinische Daten und individuelle Parameter wie Geschlecht, Alter und Vorerkrankungen in Relation zueinander und berechnen Muster für den Infektionsverlauf. PRESENt soll nicht nur individuelle Unterschiede des Norovirusinfektionsverlaufs aufdecken, sondern vor allem eine personalisierte Prognose, Prävention und Behandlung von schweren Norovirusverläufen ermöglichen.
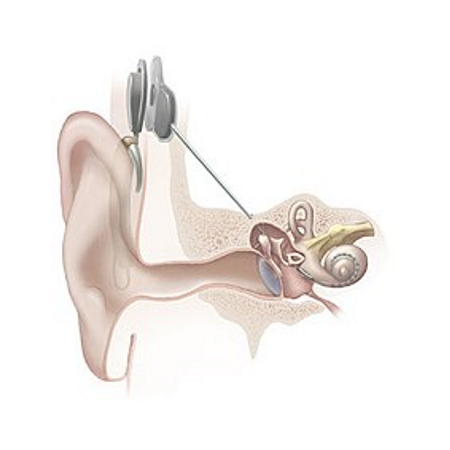
Big Data für Cochlea-Implantate
Cochlea-Implantate (CI) sind Hörprothesen für schwerhörige Patienten, bei denen konventionelle Hörgeräte keine ausreichende Verbesserung des Hörvermögens erzielen können. Das Hörvermögen nach einer CI Implantation kann jedoch stark zwischen einzelnen Patienten variieren. Da es sich hierbei um einen invasiven Eingriff handelt, haben die Patienten und behandelnde Ärzte ein Interesse daran, die Erfolgswahrscheinlichkeit vor der Operation möglichst genau abschätzen zu können.
Bisherige Anstrengungen zur Vorhersage der Prognose nach einer CI-Operation erschöpfen sich in der Untersuchung von Datensätzen, die zum einen in der Anzahl der untersuchten Patienten und zum anderen in der Vielfalt der untersuchten Daten sehr beschränkt sind. Daher lieferten entsprechende Vorhersage-Modelle bisher selten signifikante und teils sogar widersprüchliche Ergebnisse. Zudem verwenden einige Ansätze Daten, welche erst nach der Implantation vorliegen und somit keine Vorhersage vor der Entscheidung über den Eingriff ermöglichen. Somit gibt es aktuell noch kein Vorhersage-Modell, welches zur klinischen Anwendung kommt.
Zur Entwicklung eines besseren Vorhersage-Modells arbeiten wir eng mit dem Deutschen HörZentrum (DHZ) an der Medizinischen Hochschule Hannover und Forschern der Technischen Universität Braunschweig zusammen. Als weltweit größtes Kompetenzzentrum für Cochlea-Implantationen, kann uns das DHZ einen umfangreichen Datensatz von über 7.800 Patienten zur Verfügung stellen. Wir analysieren eine breite Vielfalt an verschiedenen Datentypen um aus klinischen Daten, genetischen Daten, Bildmaterial von CT Scans und Analysen von Stoffwechselprodukten diejenigen Parameter zu identifizieren, welche den größten Einfluss auf den Hörerfolg nach der CI Implantation haben. Hierbei verwenden wir ausschließlich Informationen, die auch tatsächlich vor dem Eingriff vorliegen. Mithilfe dieser Charakteristika trainieren wir ein Machine Learning Modell, das den Hörerfolg individuell für den jeweiligen Patienten vorhersagt. Das Modell wird in eine Anwendung eingebunden, die den Einsatz in der Klinik ermöglicht. In enger Zusammenarbeit mit dem DHZ integrieren wir Anforderungen wie Transparenz und Interpretierbarkeit in die Anwendung und erstellen außerdem gemeinsame Standards zur Datenerhebung um zukünftige Datenanalysen zu verbessern. Die Vorhersagen des Modells helfen den Medizinern eine maßgeschneiderte Therapie für schwerhörige Patienten zu planen und können direkt vor Ort im DHZ zum Einsatz kommen.


